Guideline
Mikrohämaturie
Zuletzt revidiert: 04/2022 Letzte Änderung: 04/2022
Aktualisierung 04/2022
- Die Guideline wurde vollständig durchgesehen und auf Aktualität geprüft
- Ein Abklärungs-Algorithmus wurde neu entwickelt (–> s. Anhang).
1. Definition (1–3)
- Als Mikrohämaturie wird eine nicht mit blossem Auge sichtbare Hämaturie bezeichnet
- Es gibt keine einheitliche Definition. Zumeist werden heute ≥ 3 Ec/GF als diagnostische Richtwerte angegeben (1–3).
2. Epidemiologie (1–6)
- Das Auftreten einer Mikrohämaturie ist ein häufiges Problem in der Allgemeinmedizin. Je nach Studienpopulation (Alter, Risikofaktoren) und Definition kommt Mikrohämaturie bei bis zu 50 % (!) vor
- Bei durch Screening erkannter asymptomatischer Mikrohämaturie beträgt die Inzidenz einer ernsthaften Erkrankung (z. B. Tumor) < 2,0 % (4, 5)
- Bei Patienten < 45 J. ist ein Urothelkarzinom sehr selten, mit zunehmendem Alter steigt die Inzidenz (12)
- Bei Jüngeren muss auch an eine asyptomatische Urolithiasis gedacht werden
- Insbesondere bei jungen Menschen ist die Mikrohämaturie häufig passager.
3. Ursachen und Bedeutung (1–4, 7, 8)
- In vielen Fällen, insbesondere bei jungen Menschen, lässt sich eine Ursache nicht eindeutig feststellen
- Eine vorübergehende Mikrohämaturie kann verschiedene Ursachen haben, am häufigsten Harnwegsinfektion, Sport, Geschlechtsverkehr
- Eine artifizielle Mikrohämaturie kann durch Menstruationsblut oder Rhabdomyolyse mit Myoglobulinurie verursacht werden
- Eine persistierende Mikrohämaturie kann urologische oder nephrologische Ursachen haben
- Das Ausmass der Mikrohämaturie lässt keine Aussage über die Ursache zu: Eine leichtgradige Mikrohämaturie schliesst eine schwerwiegende Erkrankung nicht sicher aus und eine höhergradige Mikrohämaturie weist eine solche nicht zwingend nach (12)
- Blasentumoren (Urothelkarzinom) sind die häufigste Neoplasie (bei > 60-Jährigen mit RF bis 10 %), gefolgt vom Nierenzellkarzinom (Hypernephrom) und den eher seltenen Urotheltumoren des oberen Harntraktes (Nierenbecken oder Ureter), in der Häufigkeit von etwa 100:10:1.
4. Ist ein Screening sinnvoll? (1–4, 17)
- Ein Screening bei asymptomatischen Patienten ohne RF soll nicht durchgeführt werden, da die Sensitivität dieser Testmethode für eine behandlungsbedürftige Erkrankung sehr gering ist. Die Prävalenz einer asymptomatischen malignen Erkrankung im Frühstadium beträgt < 2 %
- Bei Patienten > 45 J. mit Risikofaktoren (s. Tabelle 1) kann ein UST (Urinstix) gemacht werden, derzeit gibt es aber keine Evidenz für potentiellen Nutzen und Schaden (17).

Hinweis: In einer prospektiven Kohortenstudie erwiesen sich als Hauptrisikofaktoren: Alter > 50 Jahre,
männliches Geschlecht und Makrohämaturie. Raucheranamnese und eine hohe Ec-Zahl im Urinsediment zeigen
demnach nur ein marginal erhöhtes Neoplasma-Risiko an (15).
5. Wie zuverlässig sind Urinstreifentest und Urinsediment (Mikroskopie)?
- UST führen sehr selten zu falsch-negativen Testergebnissen
- UST reagieren entsprechend 1–2 Ec/Gesichtsfeld und sind so sensitiv wie eine Urinsedimentprüfung, haben aber eine höhere falsch-positiv-Rate (z. B. durch Sperma im Urin, Myoglobinurie, oder alkalischen Urin/pH > 9) (1, 3)
- Mit der Mikroskopie können (von geübten Untersuchern) neben Erythrocyten (Ec) u. a. Ec-Zylinder und dysmorphe Ec zuverlässig festgestellt werden – als Hinweise auf eine glomeruläre Blutungsquelle.
6. Wie soll eine Mikrohämaturie abgeklärt werden? (1, 9–15)
Es existiert kein allgemein akzeptierter, evidenzbasierter Abklärungsgang (3, 10).
Folgende Fragen sind zu klären
- Gibt es eine plausible Erklärung für die Mikrohämaturie?
- Ist die Blutung passager oder persistierend?
- Handelt es sich um eine isolierte oder eine nicht isolierte Mikrohämaturie?
- Liegen Risikofaktoren für bestimmte Erkrankungen, insbesondere Malignome (s. Tabelle 1), vor?
- Differentialdiagnosen erwägen und abfragen
- Pyurie und Dysurie –> Harnwegsinfekt (können aber auch bei Blasen-Ca vorkommen)
- Durchgemachter Atemwegsinfekt –> postinfektiöse Glomerulonephritis oder IgA-Nephropathie
- Einseitiger Flankenschmerz (ev. in die Leiste ausstrahlend) –> Nieren- oder Ureterstein
- Starke körperliche Belastung oder Nieren-/Blasen-Trauma
- Medikamenteneinnahme
- Niereninsuffizienz, Hypertonie, Diabetes meliitus
- Reise in Schistosoma-Endemiegebiet, Flüchtlingsanamnese (z. B. gehäufte Inzidenz bei eritreischen Patienten)
- Familienanamnese renale Erkrankung –> B. Polyzystische Niere.
Weiteres Vorgehen (–> vgl. Abbildung im Anhang)
- Bestätigungsmessung
- Ein positiver Befund sollte in einer zweiten Urinprobe bestätigt werden (nach 3 Tagen sexueller und sportlicher Abstinenz!). Bei hohem Risikoprofil kann auf eine Wiederholungsmessung verzichtet werden (13).
- Urinsediment
- Wird empfohlen zur Bestätigung des UST sowie zur DD glomeruläre oder nicht-glomeruläre (isomorphe) Mikrohämaturie (Tabellen 2 und 3)
- Wenn kein sauberer Mittelstrahlurin gewonnen werden kann, wird die Kontrolle mittels eines Katheterurins empfohlen
- Eine Mikrohämaturie liegt vor, wenn im Sedimen ≥ 3 Ec/GF gefunden werden
- Eine glomeruläre Mikrohämaturie ist bei Proteinurie, Ec-Zylindern, dysmorphen Ec (mehr als 5 % der Ec) sehr wahrscheinlich.


* Es gibt eine physiologische Erythrozyturie in den Primärurin. Diese liegt unterhalb der definierten Ec-Zahl für eine Mikrohämaturie, z. T. können UST aber bereits positiv reagieren

Hinweis: Antikoagulantientherapie reicht nicht als Erklärung für eine Mikrohämaturie (1, 3, 16).
- Bei älteren Frauen mit genitaler Atrophie treten Mikrohämaturien gehäuft auf. Folgendes Vorgehen kann gewählt werden
- Wenn kein spontaner sauberer Mittelstrahlurin möglich ist* –> Katheterisierung
- Topische Behandlung der lokalen Atrophie (mit Beschwerden) z. B. mit Estriol (Oestro-Gynaedron® Vag Creme oder Blissel® Vag Gel)
- Besteht nach topischer Therapie weiterhin eine (ungeklärte) Mikrohämaturie
–> urogynäkologische Abklärung.
* Hinweis: Auch bei adipösen Frauen jeglichen Alters ist die Gewinnung eines nicht kontaminierten Mittelstrahlurins schwierig.
- Urinkultur
- Bei Verdacht auf einen HWI (zusätzlicher Nachweis von Lc oder Nitrit!) –> Urinkultur mit ggfls. anschliessender Antibiotika-Therapie.
- Differenzierung isolierte oder nicht isolierte Mikrohämaturie
- Eine isolierte Mikrohämaturie besteht, wenn keine glomeruläre, infektiöse oder anders zu erklärende Blutungsursache gegeben ist (Zusammenfassung s. Tabelle 4).
7. Wann sollen Verlaufskontrollen erfolgen? (1, 3)
- Patienten mit passagerer Mikrohämaturie müssen nicht nachkontrolliert werden, solange keine Symptome auftreten
- Bei Patienten mit persistierender Mikrohämaturie und kompletter Abklärung (ohne pathologischen Befund) sind weitere Kontrollen nicht mehr erforderlich.
8. Literatur
- Perazella MA, O’Leary MP: Etiology and evaluation of hematuria in adults. UpToDate 03/2022.
- Cohen RA, et al.: MicroscopicHematuria. N Engl J Med 2003;348:2330-2338.
- Pasch A: Mikrohämaturie – Sinnvolles Vorgehen im Alltag. Swiss Medical Forum 2015;15(35):764–768.
- Jung H, Gleason JM, Loo RK, Patel HS, Slezak JM, Jacobsen SJ: Association of hematuria on microscopic urinanalysis and risk of urinary tract cancer. J Urol 2011;1698-1703.
- Hiatt RA, Ordoñez JD: Dipstick urinalysis screening, asymptomatic microhematuria, and subsequent urological cancers in a population-based sample. Cancer Epidemiol Biomarkers Prev1994;3:439-43.
- Froom P, Ribak J, Benbassat: Significance of microhaematuria in young adults. J Br Med J (Clin Res Ed). 1984;288(6410):20.
- Woolhandler S, et al.: Dipstick urinalysis screening of asymptomatic adults for urinary tract disorders. I. Hematuria and proteinuria.JAMA1989;262(9):1214.
- Mohr DN, et al.: Asymptomatic microhematuria and urologic disease. A population-based study. JAMA. 1986;256(2):224.
- Hüppe P, Wawroschek F: Methodik und aktueller Stellenwert der Mikrohämaturiediagnostik Urologe 2011;50:287.
- Rodgers M, et al.: Diagnostic tests and algorithms used in the investigation of haematuria: systematic reviews and economic evaluation Health Technology Assessment 2006; Vol. 10: No. 18 .
- Messing EM, et al.: Home screening for hematuria: results of a multiclinic study. J Urol 1992; 148:289.
- Grossfeld GD, et al.: Evaluation of asymptomatic microscopic hematuria in adults: the American Urological Association best practice policy--part I: definition, detection, prevalence, and etiology. Urology. 2001;57(4):599.
- Markart P: Mikrohämaturie: wie abklären? Der informierte Arzt 2011; 5: 20-21.
- Zellweger T: Was tun bei Hämaturie? Schweiz Med Forum 2010;10:921-923.
- Loo RK, et al.: Stratifying Risk of Urinary Tract Malignant Tumors in Patients With Asymptomatic Microscopic Hematuria. Mayo Clinic Proceedings. Volume 88, Issue 2, Pages 129–138, February 2013.
- Hurlen M, et al.: Occult bleeding in three different antithrombotic regimes after myocardial infarction. A WARIS-II subgroup analysis. Thromb Res 2006;118:433-8.
- Mayer VA, et al.: Screening for Bladder Cancer: U.S. Preventive Services Task Force Recommendation Statement. Ann Intern Med. 2011;155:246-251.
9. Anhang
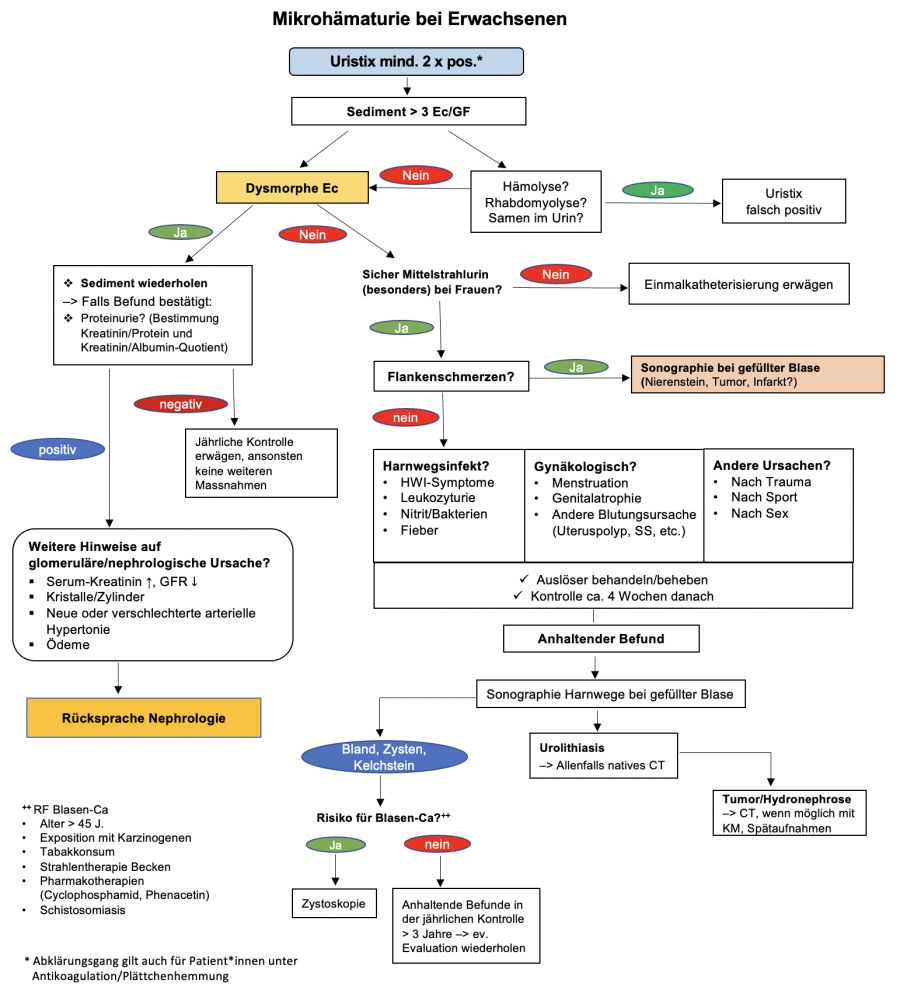
Abbildung: mediX Abklärungsalgorithmus bei Mikrohämaturie (2022)
Abkürzungen: Ec = Erythrozyten, SS = Schwangerschaft, RF = Risikofaktoren,
CT = Computertomographie, GFR = Glomeruläre Filtrationsrate
10. Impressum
Diese Guideline wurde im April 2022 aktualisiert.
© Verein mediX schweiz
Herausgeberin
PD Dr. med. Corinne Chmiel
Redaktion (verantwortlich)
Dr. med. Uwe Beise
Dr. med. Felix Huber
Dr. med. Maria Huber
Autoren
Dr. med. Felix Huber
PD Dr. med. Corinne Chmiel
Dr. med. Hartmut Knönagel
Rückmeldungen bitte an:
Diese Guideline wurde ohne externe Einflussnahme erstellt. Es bestehen keine finanziellen oder inhaltlichen Abhängigkeiten gegenüber der Industrie oder anderen Einrichtungen oder Interessengruppen.
mediX Guidelines enthalten therapeutische Handlungsempfehlungen für bestimmte Beschwerdebilder oder Behandlungssituationen. Jeder Patient muss jedoch nach seinen individuellen Gegebenheiten behandelt werden.
mediX Guidelines werden mit grosser Sorgfalt entwickelt und geprüft, dennoch kann der Verein mediX schweiz für die Richtigkeit – insbesondere von Dosierungsangaben – keine Gewähr übernehmen.
Der Verein mediX schweiz ist ein Zusammenschluss von Ärztenetzen und Ärzten in der Schweiz.
Verein mediX schweiz, Sumatrastr. 10, 8006 Zürich.